Elektron-eletron dalam atom terikat oleh gaya elektrostatik terhadap inti. Elektron-elktron ini bergerak pada lintasan tertentu yang dibolehkan. Lintasan ini terkadang disebut orbit, atau kulit, yang mengelilingi inti. Sedangkan energi elektron dalam inti adalah konstan.
Elektron pada kuliat terdalam memiliki tingkat energi yang lebih rendah dibandingkan energi elektron pada kuliat yang lebih luar. setiap kuliat hanya dapat diisi oleh sejumlah elektron, kulit terdalam (kulit yang paling dekat dnegan inti) hanya dibolehkan untuk diisi oleh dua buah elektron, dan kuliat setelahnya hanya dapat di isi oleh 8 buah elektron.
Setiap atom memiliki jumlah elektron yang berbeda. Contohnya: atom helium memiliki 2 elektron. Pada kulit terdalam, sehingga atom helium memiliki dua buah elekron pada kulit terdalam, atau memiliki tingkat energi terendah.
Tingkat energi terendah dalam atom disebut ground state. ketika atom pada ground state menyerap energi, maka satu elektron akan berpindah ke kulit yang memiliki tingkat energi lebih tinggi. sehingga atom saat ini berada dalam keadaan tereksitasi, exitated state.
Kita dapat menggunakan nilai energi eksitasi untuk meng konstruk level energy untuk atom, seperti gambar berikut:
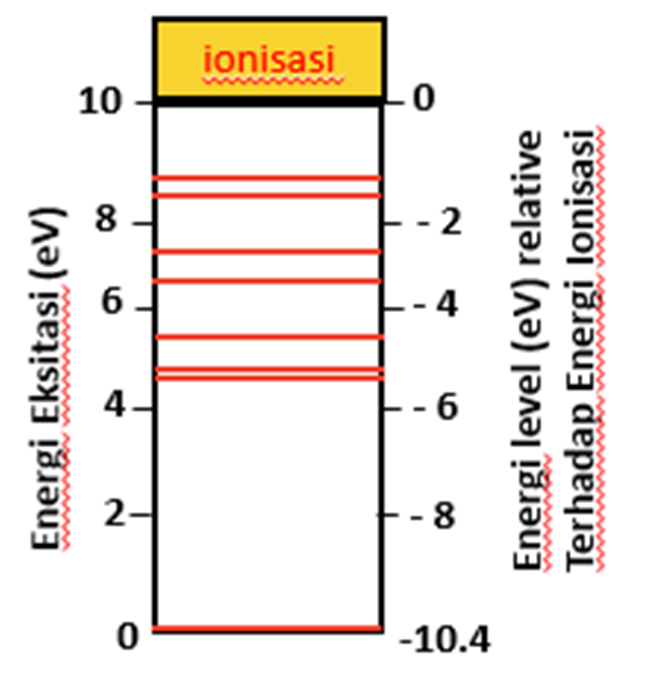
Gambar diatas menunjukkan nilai energi yang dibileh untuk atom. setiap tingkat energi yang dibolehkan berhubungan dengan konfigurasi elektron dalam atom. Kemudian setiap tingkat energi dibawah energi ionisasi diberi tanda minus. Yang memberikan arti bahwa dibutuhkan energi minimal sebesar itu untuk melepaskan elektron dari ikatan dengan inti.
De-Exitasi
Apakah anda mengetahui bahwa gas pada tekanan rendah akan mengemisikan cahaya ketika dikonduksikan listrik? Misalnya, tabung gas neon akan mengemisikan sinar orange ketika di konduksi. Pada tulisan sebelumnya tabung yang terisi gas dapat kita gunakan untuk mengukur energi eksitasi (klik disini).
sebagaimana dijelaskan pada postingan sebelumnya bahwa pristiwa eksitasi ini terjadi karena atom menyerap energi ketika proses elektron dari luar menabrak elektron dalam atom, namun atom tidak dapat mempertahankan energi yang diserap ini secara permanen atau selamanya.
Konfirgurasi elektron yang ter eksitasi dalam atom, menjadi tidak stabil karena meninggalkan kekosongan atau vacancy ketika berpindah ke kulit yang lebih luar. Cepat atau lambat, vacancy yang ditingggalkan ini akan diisi kembali oleh lektron dari kulit yang lebih luar.
ketika hal ini terjadi, elektrin yang berpindah mengemisikan photon. Atom kemudian dikatakan berpindah ke tingkat energi lebih rendah (proses ini disebiut de-exitasi).
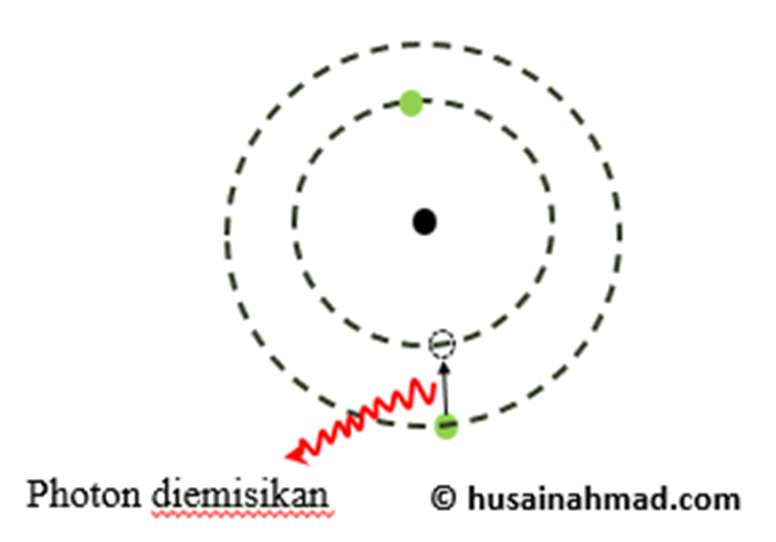
Energi photon yang diemisikan sama dengan energi yang yang hilang dari elektron. Misalnya, ketika atom merkuri pada energi eksitasi 4,9 eV de-eksitasi ke ground state, akan mengemisikan photon dengan energi sebesar 4,9 eV.
Atom mercury juga dapat melakukan de eksitasi secara tidak langsung melalui beberapa level energi jika terdapat level energi perantara. namun, jika tidak terdapat level energi antara 4,9 EV dan ground state, maka satu-satunya cara adalah dengan melakukan de-exitasi secara langsung dengan melepaskan energi photon sebesar 4,9 eV.
Secara umum, ketika elektron bergerak daei tingkat Energi E1 ke level energi lebih rendah E2.
Energi dari photon yang diemisikan hf=E1-E2.
Eksitasi Menggunakan Photon
Elektron dalam atom dapat menyerap energi photon dan berpindah ke level energi lebih tinggi (kulit lebih luar) dimana terdapat vacancy (kekosongan), namun hal ini dapat terjadi hanya jika energi photon yang diserap tepat sama dengan selesih energi dari kulit awal lektron ke kulit tempanta akan berpindah. dengan kata lain, energi photon harus sama dengan beda energi antara kedua kulit tersebut.
Jika menurut anda artikel ini bermanfaat, silahkan untuk membagikannya, memberi komentar, dan meng klik iklannya…. Hal ini dapat menjaga eksistensi website ini. Terima kasih